در دنیای امروز که بیماریهای گرمسیری نادیده گرفتهشده (NTDs) همچنان تهدیدی جدی برای سلامت عمومی به شمار میروند، پیشرفتهای علمی در حوزه تشخیص انگلها میتواند نقش کلیدی در کنترل و حذف این بیماریها ایفا کند. یکی از این پیشرفتها، توسعه حسگر زیستی DNA برای تشخیص شیستوزوما ژاپونیکوم است که اخیراً در مجله Communications Biology از انتشارات Nature منتشر شده است.
این مطالعه، که در تاریخ ۳۰ اوت ۲۰۲۵ (۹ شهریور ۱۴۰۴) به چاپ رسیده، بر اساس فناوری نوین “SNAILS” (Specific Nucleic Acid Ligation for the detection of Schistosomes) بنا شده و میتواند تحولی در تشخیص گونههای انگل شیستوزوما ایجاد کند. در این پست، به بررسی دقیق این مقاله میپردازیم و اهمیت آن را در زمینه انگلشناسی پزشکی، کنترل شیستوزومیازیس و کاربردهای آینده تشریح میکنیم.
شیستوزومیازیس: یک بیماری جهانی با عواقب سنگین
شیستوزومیازیس، که اغلب به عنوان یک بیماری گرمسیری نادیدهگرفته شده شناخته میشود، توسط انگلهای ترماتود از جنس شیستوزوما ایجاد میشود. طبق آمار سازمان بهداشت جهانی (WHO)، بیش از ۲۵۰ میلیون نفر در سراسر جهان به این بیماری مبتلا هستند و حدود ۷۷۹ میلیون نفر دیگر در معرض خطر ابتلا قرار دارند.
بار جهانی این بیماری در سال ۲۰۲۱ حدود ۲.۱۹ میلیون سال عمر تعدیلشده با ناتوانی (DALYs) برآورد شده است. به عبارت دیگر، این بیماری در مجموع معادل ۲.۱۹ میلیون سال از عمر سالم انسانها را در سطح جهان از بین برده است. شیستوزومیازیس نه تنها دومین بیماری انگلی کشنده در انسانها پس از مالاریا است، بلکه در کشورهای با درآمد پایین و متوسط (LMICs) مانند آفریقا، شبهجزیره عربستان، آمریکای جنوبی، چین، فیلیپین، اندونزی و حتی اخیراً جزیره کرس در جنوب اروپا شیوع دارد.
شیستوزوما ژاپونیکوم، یکی از گونههای اصلی این انگل است که باعث شیستوزومیازیس رودهای میشود و ویژگی زئونوتیک (قابل انتقال بین انسان و حیوان) آن، کنترل بیماری را پیچیدهتر میکند. این انگل بیش از ۴۰ گونه حیوانی خانگی و وحشی را به عنوان میزبان نهایی میپذیرد و عمدتاً در چین، فیلیپین و اندونزی یافت میشود. ژاپن در دهه ۱۹۹۰ موفق به حذف این بیماری شد، اما در سایر مناطق همچنان چالش برانگیز است.
چرخه زندگی این انگل شامل مراحل غیرجنسی در حلزونهای آب شیرین از جنس آنکوملانیا و تولید مثل جنسی در میزبان های نهایی مانند انسان است. تخم های انگل از طریق مدفوع دفع میشوند، در آب به میراسیدیوم تبدیل شده، حلزونها را آلوده میکنند و سپس سرکاریاها آزاد میشوند و از طریق پوست میزبان نفوذ کرده و آن را آلوده می کنند و سپس در بدن آن به بلوغ می رسند.
شدت بیماری زایی بالای شیستوزومیا ژاپونیکوم به دلیل تعداد بالای تخمهای تولید شده توسط آن است. کنترل این بیماری از دهه ۱۹۵۰ در چین با روشهایی مانند کنترل حلزونها، درمان دارویی جمعی و مداخلات بهداشتی انجام شده است. با این حال، تشخیص سریع و دقیق انگل در نمونههای انسانی، حیوانی، حلزونی و محیطی (مانند آب شیرین) کلیدی برای شکستن چرخه انتقال است. فناوریهای سنتی مانند روش میکروسکوپی کاتو-کاتز یا ELISA محدودیتهایی مانند دقت پایین در شیوع کم دارند. اینجا است که فناوریهای مولکولی مانند حسگر زیستی DNA وارد میدان میشوند.

معرفی فناوری SNAILS: حسگر زیستی DNA برای تشخیص گونهای شیستوزوما
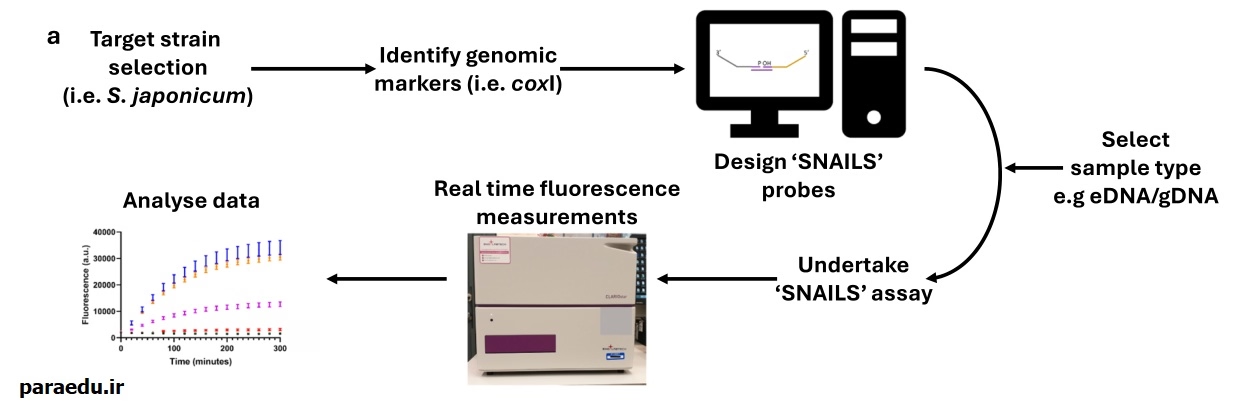
مقاله مورد بحث، که توسط تیمی از محققان به رهبری الکساندر جی. وب و پل اس. فریمنت نوشته شده، بر توسعه و اعتبارسنجی حسگر زیستی SNAILS برای تشخیص اختصاصی شیستوزوما ژاپونیکوم تمرکز دارد. SNAILS مخفف “Specific Nucleic Acid Ligation for the detection of Schistosomes” است و بر پایه یک سیستم آپتامر “Spinach” نورانی کننده بنا شده که قبلاً برای تشخیص miRNAهای سرطانی و SARS-CoV-2 استفاده شده بود.
این حسگر زیستی DNA شامل دو پروب A و B است که هر کدام نیمی از یک توالی ۲۲ بازی ssDNA هدف را شناسایی میکنند. پروب A دارای انتهای ۵’ فسفریله است و پروب B دارای انتهای ۳’ هیدروکسیله. اگر پروبها به هدف متصل شوند، لیگاز T4 DNA پیوند کووالانتی ایجاد میکند. سپس، با افزودن پروموتر T7 و RNA پلیمراز T7، آپتامر Spinach رونویسی شده و با فلوروژن DFHBI-1T ترکیب میشود تا سیگنال فلورسانس در ریل تایم تولید کند. برای افزایش اختصاصیت، پروبها در محل اتصال لیگاسیون حداکثر واگرایی توالی هدف را دارند.
در این مطالعه، هدف ژن میتوکندریایی cytochrome c oxidase subunit 1 (cox1) انتخاب شده است. با استفاده از نرمافزار MUSCLE، توالیهای cox1 از گونههای مختلف شیستوزوما همتراز شده و چهار توالی تارگت اختصاصی شیستوزوما ژاپونیکوم شناسایی شدند. این نقاط با توالی نمونه هایی از چین، فیلیپین، ژاپن و تایوان اعتبارسنجی شدند تا پوشش جغرافیایی گستردهای داشته باشند.
نتایج مطالعه: اعتبارسنجی پروبهای اختصاصی
غربالگری اولیه پروبها
چهار نوع پروب از حسگر زیستی DNA طراحی و علیه تارگت های ۲۲ نوکلئوتیدی شیستوزوما ژاپونیکوم و گونههای دیگر (مانند شیستوزوما منکونگی، مالاینسیس، مانسونی، روداینی، هماتوبیوم، بوویس، گینهانسیس و کوراسونی) آزمایش شدند. پروبهای ۲ و ۵ کاملاً اختصاصی بودند و هیچ واکنش متقاطعی نشان ندادند. پروب ۴ کمی واکنش متقاطع با شیستوزوما منکونگی داشت و پروب ۳ کمترین اختصاصیت را نشان داد.
تشخیص ssDNA مشتق از PCR
یک قطعه ۴۴۶ بازی cox1 شامل اهداف کلون شده و به عنوان کنترل استفاده شد. ssDNA با PCR اگزونوکلئاز لامبدا تولید شد. پروبهای ۲ و ۵ ssDNA را تشخیص دادند، اما پروب ۲ خروجی فلورسانس بالاتری داشت.
تشخیص نمونههای واقعی سرکاریا
پروب ۲ علیه ۱۶ نمونه سرکاریای شیستوزوما ژاپونیکوم از چین و ۳ نمونه شیستوزوما مانسونی آزمایش شد. پروب تمام نمونههای شیستوزوما ژاپونیکوم را تشخیص داد اما نمونههای مانسونی را تشخیص نداد. توالیها تأیید و در European Nucleotide Archive ثبت شدند.
بحث: اهمیت و کاربردهای آینده حسگر زیستی SNAILS
این مطالعه نشان میدهد که حسگر زیستی DNA و SNAILS میتواند سه گونه اصلی شیستوزوما (مانسونی، هماتوبیوم و ژاپونیکوم) را تشخیص دهد. تمرکز بر نمونههای محیطی مانند سرکاریا، پتانسیل آن برای نظارت محیطی را برجسته میکند SNAILS .میتواند تغییرات کوچک مانند SNPها را تشخیص دهد، که برای نظارت بر مقاومت دارویی به داروهایی مانند اکسامنیکوئین و پرازیکوانتل مفید است.
روشهای سنتی مانند کاتو-کاتز یا ELISA محدودیتهایی دارند، اما فناوریهای مولکولی مانند PCR، qPCR، LAMP و eDNA پیشرفتهایی ارائه میدهند. SNAILS با قابلیت تشخیص چندگونهای و حساسیت بالا، میتواند بخشی از پنل تشخیصی WHO باشد. این فناوری قابل گسترش به RNA با لیگاز SplintR و تشخیص پاتوژنهای دیگر است.
نتیجهگیری: گامی به سوی حذف شیستوزومیازیس
توسعه حسگر زیستی DNA SNAILS برای شیستوزوما ژاپونیکوم، پیشرفتی کلیدی در انگلشناسی پزشکی است که میتواند به کنترل بیماری در مناطق اندمیک کمک کند. با تمرکز بر تشخیص اختصاصی و سریع، این فناوری نه تنها برای تحقیقات، بلکه برای برنامههای بهداشت عمومی مانند MDA و WASH مفید است.
 انگل شناسی پزشکی Medical Parasitology
انگل شناسی پزشکی Medical Parasitology





